Mit der Schmelzenergie befassen wir uns in diesem Artikel. Dabei erklären wir, was man unter der Schmelzenergie versteht und wie man sie berechnet. Dieser Artikel gehört zum Bereich Thermodynamik.
Erhitzt man Wasser, so verdampft es bei 100 Grad Celsius ( Normaldruck ) bzw. beim Kühlen wird es bei 0 Grad Celsius ( Normaldruck ) zu Eis. Die Temperaturen für die Übergänge zwischen fest, flüssig und gasförmig sind für jeden Stoff anders und können entsprechenden Tabellen entnommen werden. Diese drei Zustände werden auch als Aggregatzustände bezeichnet.
Prinzipiell gilt: Die Wärme, die man zum Schmelzen braucht, wird beim Erstarren wieder frei. Somit ist die Schmelzenergie und die Erstarrungswärme gleich groß. Während des Schmelzens und des Erstarrens ändert sich die Temperatur der Stoffe nicht. Die Schmelzenergie berechnet sich mit der folgenden Formel:
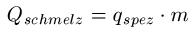
Dabei ist:
- "Qschmelz" ist die Schmelzenergie in KiloJoule [ kJ ]
- "qspez" ist die spezifische Schmelzwärme in KiloJoule pro Kilogramm [ kJ / kg ]
- "m" ist die Masse in Kilogramm [ kg ]
Beispiel:
Eine Masse von 2kg Eisen wird geschmolzen. Wie groß ist die Schmelzenergie?
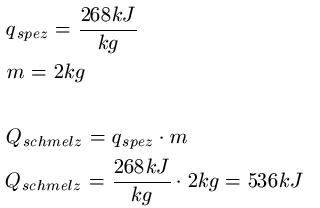
Die Schmelzenergie für 2kg Eisen beträgt demnach 536.000 Joule.
Links:
340 Gäste online
Anzeige:
Anzeige:
Verfügbare Fächer:
Anzeige:
Anzeige:
