Mit dem Aggregatzustand befassen wir uns in diesem Artikel. Dabei wird erklärt, welche Aggregatzustände es gibt und welche Eigenschaften dann vorliegen. Dieser Artikel gehört zum Bereich Thermodynamik.
Mit dem Begriff Aggregatzustand bezeichnet man den physikalischen Zustand eines Stoffes. Es gibt drei klassische Aggregatzustände: Fest, flüssig und gasförmig. Welcher Aggregatzustand vorliegt, hängt von den Eigenheiten des Stoffes, der Temperatur und dem Druck ab.
Aggregatzustand fest:
In den meisten Fällen kann man sagen, dass Stoffe im Aggregatzustand "fest" die größte Dichte besitzen, welche etwa 5-10 Prozent höher als die der jeweiligen Flüssigkeit ist. Wirkt keine äußere Kraft auf den Stoff ein, behält er seine Form bei.
Aggregatzustand flüssig:
Im flüssigen Zustand hingegen, passt sich der Stoff in seiner Form der Umgebung an. Beispiel: Kaffee passt sich der Form der Innenwände eines Glases an und fließt immer zum tiefsten Punkt. Dies gilt auch in der Natur: Flüsse fließen stets den Berg runter.
Aggregatzustand gasförmig:
Nach fest und flüssig fehlt nun noch der Aggregatzustand "gasförmig". Erhitzt man eine Flüssigkeit sehr stark, wird sie irgendwann verdampfen, sprich sie "geht in die Luft über". Als Gas weisen die Stoffe die niedrigste Dichte auf. Diese ist bis zu tausendmal kleiner als die der Feststoffe. Aus diesem Grund kann man gasförmige Stoffe auch sehr stark komprimieren. In diesem Aggregatzustand besitzt der Stoff keine fest Oberfläche. Deshalb sind farblose Gase unsichtbar.
Zur Grafik: Im festen Zustand haben die Teilchen der Stoffe einen festen Platz um den sie "schwingen". Im flüssigen Zustand ist dies nicht mehr der Fall, sondern die Teilchen sind gegeneinander verschiebbar. Im gasförmigen Zustand können sich die Teilchen frei bewegen.
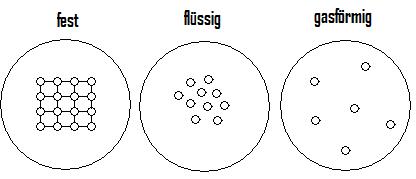
Aggregatzustand: Teilchenmodell
In der Thermodynamik wird regelmäßig mit so genannten Modellen gearbeitet. Dabei handelt es sich um eine "Vorstellung" davon, wie man sich bestimmte Aufbauweisen und Eigenschaften klar machen kann. Modelle sollen Menschen helfen, sich viele Dinge besser vorstellen zu können. Um die Eigenschafen von Feststoffen, Flüssigkeiten und Gasen etwas besser beschreiben zu können, zeigen wir euch hier das Teilchenmodell.
Beim Teilchenmodell geht man davon aus, dass ein Stoff aus kleinen Kugeln besteht. In der Wirklichkeit sind zwar diese kleinsten Teilchen (Atome, Moleküle oder Ionen) von anderer Form, aber für die Erklärung der drei Aggregatzustände reicht es aus, die Teilchen als kleine, runde Kugeln anzusehen.
Die Bewegung der Teilchen der drei Zustände ist ein Maß für die Temperatur des Stoffes. Die Art der Bewegung ist in den drei Aggregatzuständen jedoch völlig unterschiedlich. Im Gas bewegen sich die Teilchen geradlinig ( so wie z.B. Billardkugeln ), bis sie mit einem anderen oder mit der Gefäßwand zusammen stoßen. In der Flüssigkeit müssen sich die Teilchen durch Lücken zwischen ihren Nachbarn hindurch zwängen. Im Festkörper bewegen sich die Teilchen nur wenig um ihre Ruhelage.
Links:
167 Gäste online
Anzeige:
Anzeige:
Verfügbare Fächer:
Anzeige:
Anzeige:
